, Martin Jung2 und Ernst Wiedemann2
(1)
Fakultät für Therapiewissenschaften, SRH Hochschule Heidelberg, 69123 Heidelberg, Deutschland
(2)
OCM Orthopädische Chirurgie München, Steinerstr. 6, 81369 München, Deutschland
Zusammenfassung
Operative Eingriffe an der oberen Extremität kommen häufig vor. Die physiotherapeutische Nachsorge sollte zügig, ökonomisch und effektiv gestaltet sein, mit dem Ziel, die volle Alltags- und Arbeitsfähigkeit des Patienten wiederherzustellen. Dies verlangt neben therapeutischer Kompetenz und Professionalität eine optimale Abstimmung zwischen Arzt und Therapeut sowie eine gute Aufklärung, Führung und Mitarbeit des Patienten. Neben einer sinnvollen Selektion der Behandlungsmaßnahmen trägt außerdem ein zeitlich gut geplanter Einsatz dieser Maßnahmen zum Erfolg bei. In diesem Kapitel wird zuerst auf die Ziele und Prinzipien der physiotherapeutischen Nachbehandlung eingegangen, folgend werden die chirurgischen Eingriffe für die verschiedenen Pathologien dargestellt sowie die entsprechende physiotherapeutische Nachbehandlung exemplarisch aufgezeigt.
7.1 Postoperative Rehabilitation nach ausgewählten Eingriffen an der oberen Extremität
Operative Eingriffe an der oberen Extremität kommen häufig vor. Die physiotherapeutische Nachsorge sollte zügig, ökonomisch und effektiv gestaltet sein, mit dem Ziel, die volle Alltags- und Arbeitsfähigkeit des Patienten wiederherzustellen. Dies verlangt neben therapeutischer Kompetenz und Professionalität eine optimale Abstimmung zwischen Arzt und Therapeut sowie eine gute Aufklärung, Führung und Mitarbeit des Patienten. Neben einer sinnvollen Selektion der Behandlungsmaßnahmen trägt außerdem ein zeitlich gut geplanter Einsatz dieser Maßnahmen zum Erfolg bei.
In diesem Kapitel wird zuerst auf die Ziele und Prinzipien der physiotherapeutischen Nachbehandlung eingegangen und im Weiteren eine exemplarische Übersicht über den Rehabilitationsaufbau und die Rehabilitation der Gelenksteuerung gegeben.
Danach wird das chirurgische Vorgehen bei ausgewählten, häufig vorkommenden operativen Eingriffen an Schulter, Ellenbogen und Hand dargestellt. Jeweils anschließend an diese Darstellungen werden dann die Besonderheiten bei der Nachbehandlung der einzelnen Eingriffe beschrieben. In ◘ Tab. 7.2, 7.5 und 7.7 ist jeweils eine Übersicht über den Nachbehandlungsablauf mit den wichtigsten Zielen, Einschränkungen und Schwerpunkten der einzelnen Phasen dargestellt. Diese allgemeingültigen Übersichten sollten an den einzelnen Patienten und seine individuelle Situation angepasst werden.
Die zur Nachbehandlung notwendigen Techniken sind in den vorangegangenen Kapiteln bereits ausreichend dargestellt worden, so dass sie in diesem Kapitel nicht mehr wiederholt werden.
7.1.1 Zielsetzung
Ziel des operativen Eingriffs und der anschließenden Rehabilitation ist es, die vollständige Funktionsfähigkeit des Patienten wiederherzustellen. Hierzu ist es notwendig, das volle schmerzfreie passive und aktive Bewegungsausmaß sowie die volle Kraft und Kontrolle wiederzuerlangen. Da dies abhängig von der Ausgangssituation und Vorgeschichte des Patienten nicht immer möglich ist, wird eine bestmögliche Funktion angestrebt. Eine realistische Prognose und Zielsetzungs sollte hier mithilfe der ICF der WHO erarbeitet werden.
7.1.2 Allgemeine Kriterien und Prinzipien
Bei der postoperativen Rehabilitation ist die Berücksichtigung der folgenden Kriterien und Prinzipien wichtig:
Wundheilungsverlauf
Da durch den operativen Eingriff ein klarer Startpunkt gesetzt worden ist, können die Wundheilungsphasen als wichtige Leitschnur dienen, um die Belastungen, Behandlungsmaßnahmen und -intensitäten an die spezifischen Bedürfnisse des heilenden Gewebes anzupassen und somit den Heilungsverlauf optimal zu unterstützen. Ein Überblick über die Wundheilungsphasen und deren Konsequenz für die Therapie ist in ◘ Abb. 2.3 dargestellt.
Immobilisationszeiten
Häufig ist es notwendig, die operativ versorgten Strukturen in der ersten postoperativen Phase ruhigzustellen und zu entlasten, um ihnen Zeit zur Heilung und Festigung zu geben. Die Entlastungsdauer wird i. d. R. vom Operateur auf Grundlage des intraoperativen Befunds und seiner Erfahrung festgelegt. Im Laufe der letzten Jahre haben sich die Immobilisationszeiten eher verkürzt, was sich in vielen Fällen positiv auf den therapeutischen Gesamtprozess und die Kosten ausgewirkt hat. Die therapeutischen Limitierungen für die Nachbehandlung nach operativen Eingriffen sind in ◘ Tab. 7.2, 7.5 und 7.7 angegeben. Allerdings besteht nach meinem Erachten noch viel Potenzial, sowohl die Erfahrungen von Physiotherapeuten und Operateuren zu vereinen als auch die Effekte unterschiedlicher Nachbehandlungsprotokolle miteinander zu vergleichen und anhand dessen die Nachbehandlungsschemata zu optimieren.
Tab. 7.1
Einteilung der AC-Gelenkverletzungen nach Rockwood
Typ | Verletzung |
|---|---|
1 | Dehnung der AC-Kapsel, intakte CC-Bänder |
2 | Zerreißung der AC-Kapsel, Dehnung der CC-Bänder, CC-Abstand bis 25 % vergrößert |
3 | Zerreißung der AC-Kapsel und der CC-Bänder, CC-Abstand 25–100 % vergrößert |
4 | Wie Typ 3, jedoch Klavikula nach dorsal in den Trapezius disloziert |
5 | Wie Typ 3, jedoch CC-Abstand 100–300 % vergrößert |
6 | Wie Typ 3, jedoch Klavikula unter das Korakoid disloziert |
(Rockwood u. Green 1984). CC-Bänder: korakoklavikuläre Bänder. CC-Abstand: korakoklavikulärer Abstand im Röntgenbild | |
Tab. 7.2
Therapeutische Limitierungen in der Rehabilitation nach operativen Eingriffen an der Schulter
Woche 1 | Woche 2 | Woche 3 | Woche 4 | Woche 5 | Woche 6 | Woche 7 | Woche 8–13 | |
|---|---|---|---|---|---|---|---|---|
Subakromiale Depression | – pMOB der FLEX bis zur Schmerzgrenze – Ø aBEW gegen WST – Ø aBEW | Siehe Woche 1 – pMOB der FLEX und ABD bis zur Schmerzgrenze – Anbahnung der SM – Schmerzfreie aBEW unterhalb 60° FLEX/ABD | – pMOB und aBEW bis zur Schmerzgrenze (max. 90°) – Kontrollierte ADLs – Dynamische Kräftigung der SM – Isometrische Kräftigung der RM in 0-Stlg gegen leichten WST | – pMOB und aBEW bis zur Schmerzgrenze – Dynamische Kräftigung der RM in 0° ABD im eigeschränkten Bewegungsausmaß und der SM | – Schmerzfreies Üben gegen leichten WST bis 90° FLEX | Siehe Woche 5 | Siehe Woche 5 – aBEW oberhalb 90° FLEX und bis 90° ABD – Keine kombinierte ABD-AR-Bewegung bis zur 10. Woche | – Progressives Training gegen WST, auch oberhalb 90° ABD – Progressives, aber nicht forciertes Training in ABD-AR-Position |
Stabilisierung nach ventraler Schulterluxation | – Gilchrist v. a. nachts – Ø pAR – Ø aAR – Ø aIR – aaFLEX und aaABD bis 60° in 10° IR – pAR und aEXT bis 0° | Siehe Woche 1 – Anbahnen der RM und SM | – Ø pAR – aAR bis 0° – aABD und aFLEX bis 90° | Siehe Woche 3 – Statische und dynamische Stabilisation | Siehe Woche 4 – aAR bis 0° – pAR bis 20° mit ventraler manueller Sicherung | Siehe Woche 5 | – Progressive Steigerung der apBEW | – Ab Woche 8 Langsame Belastungssteigerung und KGG mit Schwerpunkt Gelenksicherung und -steuerung |
RM-Rekonstruktion | – Abduktionskissen Tag und Nacht – Ø ADD – Ø EXT – Ø aBEW – Ø aAR/aIR – pABD und pFLEX je nach Vorgaben und Schmerzintensität bis 60° | Siehe Woche 1 – Anbahnen der SM | Siehe Woche 2 – aaBEW im kleinen Ausmaß – Anbahnung der RM – pMOB der FLEX bis 90° – pIR/pAR 30–0–40° in 30° ABD-Stlg bis zur Schmerzgrenze | Siehe Woche 3 | – Abduktionskissen nach Bedarf – Progressive pMOB bis 90° FLEX und ABD – aaABD bis 90° – Geführte aAR/aIR erlaubt | Siehe Woche 5 | – Progressive Verbesserung der pMOB – aBEW ohne WST im schmerzfreien Bereich | – Ab Woche 9 BEW gegen leichten WST unter Schulterhöhe, ab Woche 11 darüber – Ab Woche 13 KGG |
Schulterprothese | – Gilchrist nachts, tagsüber nach Bedarf – Schmerzfreie pMOB und aaMOB in FLEX, ABD, ADD – Ø pAR – Ø aAR – Ø aIR (anatomische Prothese) – pAR und – paEXT bis 20° (inverse Prothese) | Siehe Woche 1 | – Gilchrist nachts und tagsüber nach Bedarf – Progressive schmerzfreie pMOB und aaMOB in FLEX, ABD, ADD, AR, EXT – Ø pAR – Ø aAR – Ø aIR (anatomische Prothese) | – Gilchrist nachts und tagsüber nach Bedarf – Schmerzfreie aBEW unter Schulterhöhe – Progressives Erweitern der pBEW | Siehe Woche 4 | – aBEW frei bis zur Schmerzgrenze | Siehe Woche 7 | – aBEW gegen leichten WST – Ab Woche 12 dosierte KGG |
ACG-Sprengung (Rockwood 3–6) | – Armschlaufe tagsüber zur Entlastung des ACG – pFLEX, pABD bis maximal 90° in Woche 1–4(6) | Siehe Woche 1 – Anbahnung der SM – Isometrische Kräftigung der RM in 0-Stlg gegen leichten WST | Siehe Woche 2 – pMOB im GHG – Anbahnung und isometrische Kräftigung der SM | Siehe Woche 3 – Dynamische Kräftigung der RM in 0° ABD im eingeschränkten Bewegungsausmaß und der SM – Aktive Bewegungen im GHG unter Schulterhöhe – Keine pMOB des ACG! | – Progressive aktive Bewegungserweiterung im Schultergürtel – Aktive Elevation bis 90° (Schmerzgrenze!) erlaubt – Kein Widerstand am langen Hebel bis Woche 10! | – Ab Woche 10 dosierte KGG | ||
p: passiv; a: aktiv; aa: aktiv-assistiv; ap: aktiv und passiv; MOB: Mobilisation; BEW: Bewegung; WST: Widerstand; Ø: keine; ABD: Abduktion; ADLs: Aktivitäten des täglichen Lebens; ADD: Adduktion; FLEX: Flexion; EXT: Extension; IR: Innenrotation; AR: Außenrotation; 0-Stlg: Nullstellung; RM: Rotatorenmanschette; SM: Skapulamuskulatur; KGG: Krankengymnastik am Gerät | ||||||||
Einflussnehmende und beitragende Faktoren
Faktoren wie beispielsweise
eine hohe Schmerzintensität,
eine starke (reflektorische) Bewegungseinschränkung sowie
Mitarbeit, Motivation und Vertrauen des Patienten zum therapeutischen Umfeld
können für den (Miss-)Erfolg der Nachbehandlung entscheidend sein. Eine entsprechende Aufklärung und Behandlung des Patienten kann diese Faktoren und somit das Ergebnis optimieren. Da die aktive Mitarbeit des Patienten einen wesentlichen Aspekt der Rehabilitation darstellt, ist in jeder Phase eine entsprechende Instruktion für das Alltagsverhalten und die Heimübungen wichtig.
7.1.3 Rehabilitation der aktiven Gelenksteuerung
Neben einer funktionellen Mobilität spielt die Qualität der aktiven Gelenksteuerung eine entscheidende Rolle für den Erfolg der Nachbehandlung. Obwohl dieser Aspekt sich in den Gesamtprozess der Rehabilitation eingliedert, werden aufgrund der Wichtigkeit die einzelnen Phasen nochmals aufgezeigt. Der Schwerpunkt liegt grundsätzlich auf einem wohl dosierten, progressiven Training
der Propriozeption,
der Ermüdungswiderstandsfähigkeit und
der statischen und dynamischen Stabilisationsfähigkeit der Muskulatur.
Außerdem wird die gesamte kinetische Kette der oberen Extremität in die Therapie miteinbezogen. Ein Beispiel für diesen Prozess findet sich in ▶ Abschn. 4.4.4, „Therapie der Schulterinstabilität: Behandlungsaufbau“.
Rehabilitationsprozess
Phase 1: Reduzieren und Beseitigen der Störfaktoren
Um die aktive Gelenksteuerung wiederherzustellen, müssen zunächst Störfaktoren wie z. B. Schmerz, Schwellung, Angst usw. beseitigt werden (s. auch ▶ Abschn. 7.1.4).
Phase 2: Muskuläre Anbahnung
Ziel dieser Phase ist es, die Muskulatur mittels bahnender Techniken wieder in ihre ursprüngliche Funktion zu bringen. Vor allem bei den traumatischen erworbenen Instabilitäten führt die Reparatur des beschädigten Gewebes durch die Operation selbst und die Beseitigung der Störfaktoren schon zu einer besseren Gelenksteuerung und Muskelfunktion, wodurch diese direkt extensiv im Ausdauerbereich beübt werden kann.
Phase 3: Statische und dynamische Stabilisation
Für die statische und dynamische Stabilisation eignen sich Übungen in der offenen und geschlossenen Kette mit oder ohne Hilfsmittel, die im Verlauf progressiv gesteigert und komplexer gestaltet werden. Der dynamische Anteil und somit auch die intermuskuläre Kontrolle tritt dadurch mehr und mehr in den Vordergrund.
Phase 4: Reaktive neuromuskuläre Kontrolle
Durch exzentrische und reaktive Impulse wird die dynamische Gelenkkontrolle im offenen und geschlossenen System verbessert.
Phase 5: Funktionelle Muster
Diese Phase entwickelt sich fließend aus Phase 4. Es werden berufs- oder sportartspezifische Muster trainiert und langsam in der Intensität gesteigert.
7.1.4 Allgemeiner Rehabilitationsaufbau
In diesem Abschnitt wird ein allgemeingültiges Nachbehandlungsschema dargestellt. Für jede einzelne Rehabilitationsphase werden die Ziele genannt und entsprechende Maßnahmen beispielhaft dargestellt. Die Maßnahmen zielen in unterschiedlicher Gewichtung auf Schmerzlinderung und Stoffwechselförderung, Mobilitätsverbesserung, Verbesserung der aktiven Gelenksteuerung und Kraft sowie Aufklärung und Instruktion des Patienten ab.
Vorsicht
Es ist zu beachten, dass alle Maßnahmen eine bestimmte Schmerzintensität von ca. 3–4/10 auf einer visuellen numerischen Skala (VNS) nicht überschreiten und nach Beendigung der Maßnahme innerhalb von wenigen Minuten wieder abklingen sollten.
Rehabilitationsphasen
Vorbereitungsphase
Der Patient sollte frühzeitig über den zeitlichen Umfang und Ablauf der Rehabilitation aufgeklärt werden, damit die entsprechenden Maßnahmen organisiert und sämtliche Termine schon präoperativ geplant werden können. Je nach persönlicher Situation kann die Nachbehandlung stationär, teilstationär oder ambulant erfolgen.
Phase 1 (Entlastungsphase)
Ziele:
Schmerzreduktion,
Kontrolle der Entzündung,
Schaffen von optimalen Bedingungen für die Wundheilung,
Erhalten der Mobilität.
Maßnahmen:
Ruhe, Entlastung, (intermittierende) Immobilisation,
Lymphdrainage,
physikalische Anwendungen,
evtl. schmerz- und entzündungshemmende Medikamente,
dynamisch-funktionelle Gelenkmobilisation im schmerz- und widerstandsfreien Bereich.
Der Einsatz einer Bewegungsschiene ist zwar umstritten, kann aber in bestimmten Fällen eingesetzt werden. Außerdem sollte eine befundorientierte Behandlung der angrenzenden Bereiche wie z. B. der HWS oder der Nackenmuskulatur erfolgen.
Phase 2 (Teilbelastungsphase)
Ziele:
Verbesserung des passiven Bewegungsausmaßes,
muskuläre Anbahnung und Tonusregulierung,
Erhalt der Beweglichkeit und Kraft der angrenzenden Gelenke, der neuralen Strukturen sowie der allgemeinen Fitness,
Schmerzfreiheit am Ende dieser Phase.
Maßnahmen:
Befundorientierte Gelenkmobilisationen,
aktiv-assistive Bewegungen für die noch zu entlastenden Strukturen,
aktive Mobilisation der freigegebenen Richtungen.
Phase 1–2 der aktiven Gelenksteuerung (▶ Abschn. 7.1.3),
Instruktion der möglichen ADLs und Heimübungen, auch z. B. zu Rumpf- und Beinkräftigung.
Vorsicht
Von einer aktiven Mobilisation im Wasser ist in dieser Phase aufgrund der Überlastungsgefahr abzuraten.
Phase 3 (Belastungsphase 1, „Alltagsbelastung“)
Ziele:
Wiederherstellen des vollen passiven Bewegungsausmaßes,
statische und dynamische Stabilität, Verbesserung der Kraftausdauer,
Wiederaufnahme der beruflichen Tätigkeit (bei leichterer körperlicher Anforderung).
Maßnahmen:
Intensive manuelle Mobilisation des betroffenen Gelenkbereichs und der angrenzenden Gelenke,
Phase 2–3 der aktiven Gelenksteuerung (▶ Abschn. 7.1.3),
Beginn eines lokalen dynamischen Kraftausdauertrainings und eines Trainings der angrenzenden, zur kinetischen Kette der oberen Extremität gehörigen Gelenke mit entsprechender Anleitung für das Heimprogramm.
Phase 4 (Belastungsphase 2, „Arbeits-/Sportbelastung“)
Ziele:
Volle Beweglichkeit,
reaktive neuromuskuläre Kontrolle, funktionelle Muster,
Wiederaufnahme der Arbeit (bei körperlich anstrengenden Berufen) und der sportlichen Belastung.
Maßnahmen:
Endgradige Mobilisation der Gelenke (falls notwendig),
Phase 4 und 5 der aktiven Gelenksteuerung (▶ Abschn. 7.1.3).
Bei körperlich schwerer Arbeit oder bei Sportarten, bei der/denen die obere Extremität stark beansprucht wird, ist ein Training zur Muskelhypertrophie, Verbesserung der intramuskulären Koordination und schließlich zur Reaktivität der gesamten kinetischen Kette notwendig.
7.2 Chirurgische Therapie häufiger Pathologien an der Schulter
7.2.1 Subakromiale Dekompression (SAD)
OP-Indikation
Die Indikation zur subakromialen Dekompression ergibt sich bei einer knöchernen Enge des Subakromialraums. Häufig wird diese Enge durch einen anterolateralen Knochensporn am Akromion bedingt, der eine schmerzhafte Bewegungseinschränkung der Schulter hervorruft. Bei strenger Indikationsstellung sollte eine konservative Therapie über 6 Monate vorausgehen, die keinen anhaltenden Erfolg erbracht hat. Das bedeutet, dass die Impingementtests auch nach dieser Behandlung positiv bleiben (Einzelheiten zu den Tests ▶ Abschn. 7.2.7).
Diagnosestellung
Folgende bildgebende Untersuchungen sollten vorliegen:
eine Standardröntgenserie in 3 Ebenen (true a.p., transskapulär, axial) und
eine MRT, um den Zustand der Rotatorenmanschette beurteilen zu können.
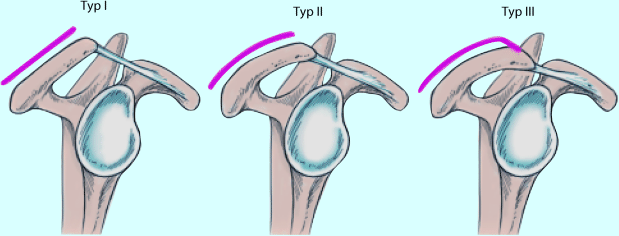
Im Röntgenbild kann das Akromion nach Bigliani und Morrison et al. (1986) in 3 Typen eingeteilt werden (◘ Abb. 7.1):
Typ 1: flach.
Typ 2: gekrümmt.
Typ 3: hakenförmig.
Ein stark gekrümmtes oder hakenförmiges Akromion drückt lokal auf die darunter liegende Rotatorenmanschette und verursacht so Schmerzen. Die Aussichten der konservativen Therapie sind bei einer solch ungünstigen Akromionform geringer als bei einem flachen Akromion.
Operatives Vorgehen
Ziel des Eingriffs ist es, den Knochensporn am Akromion abzutragen und die Form des Akromions zu normalisieren, also eine flache bis gleichmäßig gekrümmte Unterfläche herzustellen, die mit der Oberfläche der Rotatorenmanschette harmoniert (◘ Abb. 7.2). Die subakromiale Dekompression wurde früher offen durchgeführt und die Unterfläche des Akromions mit einem Meißel und einer Feile bearbeitet (Akromioplastik). Der jetzige Standard ist das arthroskopische Vorgehen.
Technik der subakromialen Dekompression
Bei der Lagerung kommt sowohl die in den USA favorisierte Seitenlagerung („lateral decubitus“) als auch die halbsitzende Lagerung („beach chair“) in Betracht. Letztlich hängt dies an der Vorliebe und Gewohnheit des Operateurs. Wichtig ist das Einzeichnen der anatomischen Landmarken auf der Hautoberfläche, um während der Operation die Übersicht zu behalten.
Der Eingriff beginnt mit einer Arthroskopie des Glenohumeralgelenks. Hierzu wird das Arthroskop über das dorsale Standardportal in das Gelenk eingebracht. Intraartikuläre Schäden am Knorpel, an den Ansätzen der Rotatorenmanschette und an der langen Bizepssehne werden systematisch eingeordnet. Kleinere Schäden können mit einem kleinen, rotierenden Weichteilresektor (Shaver) oder einer Knochenfräse behandelt werden.
Findet sich im Idealfall ein unversehrtes Gelenk, so wird das Arthroskop zurückgezogen und über dasselbe dorsale Standardportal in den Subakromialraum vorgeschoben. Dabei handelt es sich um einen anatomisch vorgeformten Raum, der zwischen den beiden Blättern der Bursa subacromialis bzw. subdeltoidea liegt. Das untere Blatt des Schleimbeutels liegt der Rotatorenmanschette auf und ist innig mit dieser verwachsen. Das obere Blatt entspricht der Unterfläche des Akromions bzw. des Deltamuskels.
Auch im Subakromialraum erfolgt zunächst eine diagnostische Einordnung der Befunde:
ist der Schleimbeutel verdickt, entzündet oder zottig?
ist der Ansatz des korakoakromialen Bandes am Akromion verdickt, entzündet oder zerfasert?
ist die Oberfläche der Rotatorenmanschette entzündet, zerfasert oder bereits teilweise eingerissen?
Der Schleimbeutel muss danach zu großen Teilen mit einem rotierenden Weichteilresektor oder mit einem elektrischen Vaporisateur entfernt werden. Das Werkzeug wird über ein zweites, seitliches Portal eingebracht, das in seitlicher Verlängerung der Mitte des Akromions angelegt wird. Die Weichteilresektion dient der Entfernung des entzündlichen und damit schmerzhaften Gewebes, der Verminderung des Gewebevolumens im Subakromialraum und nicht zuletzt der Übersicht für die eigentliche Knochenresektion. Hierzu wird der Ansatz des korakoakromialen Bandes am Akromion mit dem Weichteilresektor oder elektrisch abgelöst. Dabei muss man vorsichtig vorgehen, weil es gern zu Blutungen kommt, die lästig sind und die Übersicht erschweren. Ist der Ansatz des korakoakromialen Bandes verknöchert, wird dieser Knochensporn entfernt. Das korakoakromiale Band selbst wird belassen.
Danach wird die vordere Unterkante des Akromions mit einer kleinen Fräse begradigt. Man beginnt an der anterolateralen Kante und legt sich hier eine Marke vor, die der im Röntgenbild ausgemessenen, maximalen knöchernen Resektionshöhe entspricht. Von dieser Marke ausgehend wird das Akromion nach innen in Richtung AC-Gelenk und nach hinten eingeebnet. Die dorsale Begrenzung der Resektion entspricht der Hinterkante des AC-Gelenks. Die Übergänge zum nativen Akromion müssen gleichmäßig auslaufen.
Um die Qualität der Resektion zu überprüfen, sollten das Arthroskop und die Knochenfräse mehrfach gegeneinander ausgetauscht werden. Bei dem Vorgang handelt es sich um eine dreidimensionale Fräsung, die nur mit der Sicht aus mindestens zwei Blickwinkeln sicher zu beurteilen ist. Bei der subakromialen Dekompression kommt es letztlich nicht darauf an, wie viel Knochen entfernt wird. Wichtiger ist die perfekte Glätte der gefrästen Fläche, bei der keine Unebenheiten oder Knochenkanten an den Rändern verbleiben dürfen. Nicht zu unterschätzen ist der zusätzliche Effekt, der durch die gleichzeitige Entfernung der schmerzhaften sensiblen Endigungen im Periost des Akromions erzielt wird.
Nachbehandlung
Bei der physiotherapeutischen Nachsorge sollte zunächst die Anteversion und danach die Abduktion passiv und im schmerzfreien Bereich geübt werden. Rotationsbewegungen sind erst sinnvoll, sobald die passive Anteversion nicht mehr eingeschränkt ist, was meist einige Wochen benötigt. Gefährlich ist die aktive Belastung innerhalb der ersten Wochen, weil diese eine Kapselentzündung auslösen kann, die sich verselbständigen kann und dann Wochen benötigt, um wieder abzuklingen.
7.2.2 Rotatorenmanschette und lange Bizepssehne
Läsionen der Rotatorenmanschette
Diagnosestellung
Folgende bildgebende Untersuchungen sollten vorliegen:
eine Standardröntgenserie in 3 Ebenen (true a.p., transskapulär, axial) und
eine MRT, um den Zustand der Rotatorenmanschette beurteilen zu können.
Die Rekonstruktion der Rotatorenmanschette ist nur sinnvoll, sofern Atrophie und Verfettung des zugehörigen Muskels im Kernspintomogramm gering ausgeprägt sind!
Zur Sicherung der Diagnose werden standardisierte Tests verwendet, die eine Einschätzung des Kraft- und Funktionsverlusts erlauben. Besonders wichtig zur Beurteilung sind
der Jobe-Test: Supraspinatussehne,
der Patte-Test: Infraspinatussehne und
der Bear Hug-Test: Subskapularissehne (Einzelheiten ▶ Abschn. 7.2.7, Anhang).
Operatives Vorgehen
Die aktuelle Standardtherapie eines Schadens an der Rotatorenmanschette beinhaltet 3 Schritte:
die Arthroskopie, um Zusatzschäden abzugrenzen und die technische Rekonstruierbarkeit der Rotatorenmanschette zu sichern,
die knöcherne Erweiterung des Subakromialraums vorzugsweise in arthroskopischer Technik, um der rekonstruierten Sehne mehr Platz zu verschaffen, und
die eigentliche Sehnennaht, die offen mit transossären Nähten oder arthroskopisch mit Ankernähten erfolgt.
Operationstechnik
Sofern die eigentliche Sehnennaht offen erfolgen soll, ist die halbsitzende Lagerung („beach chair“) zu bevorzugen. In Seitenlagerung („lateral decubitus“) ist zwar eine offene Sehnennaht möglich, wegen der um 90° verdrehten Anatomie aber für den Operateur schwierig. Die arthroskopische Sehnennaht ist in beiden Lagerungsvarianten gleichermaßen möglich.
Bereits bei der Arthroskopie des Glenohumeralgelenks wird der nicht mehr vom Sehnenansatz bedeckte, freiliegende Anteil des Tuberculum majus von Sehnenresten befreit und knöchern angefrischt, bis er blutet, um die Einheilung der Sehne zu fördern, die ja ihrerseits schlecht durchblutet ist. Der häufig ausgefranste Rand der Sehne wird zurechtgeschnitten, und lockere Sehnenreste werden abgetragen.
Das Arthroskop wird danach in den Subakromialraum orientiert. Vorrangig erfolgt jetzt die subakromiale Dekompression (s. oben). Manchmal ist es besser, die Dekompression erst nach der Rekonstruktion des Sehnenansatzes auszuführen. Dies hat Vor- und Nachteile, die der individuellen Vorliebe des Operateurs entsprechen.
Wesentlich ist die Mobilisation der abgelösten Anteile der Rotatorenmanschette, die sowohl an der Sehnenoberfläche als auch an der Sehnenunterfläche erfolgen muss. Je nach Zustand der Sehnenränder und Ausmaß der Retraktion kann dieser Schritt einfach oder kompliziert sein. Am Ende der Mobilisation sollte sich der Sehnenrand bei einer Probereposition mit geringer Spannung in anatomischer Position an das Tuberculum majus anlegen lassen. Gelingt dies bei einem weit retrahierten, U-förmigen Defekt nicht, können zur Verkleinerung des Defekts zuerst quere Nähte angelegt werden. Der verkleinerte Restdefekt wird danach am Knochen befestigt (sog. Margin Convergence nach Burkhart; Burkhart et al. 1996).
Zur Rekonstruktion des Sehnenansatzes werden Anker in den freiliegenden Anteil des Tuberculum majus eingedreht. Diese Anker werden von der Industrie als Titananker und als resorbierbare Anker zur Verfügung gestellt und enthalten nicht resorbierbare Fäden, die durch den Sehnenansatz transportiert und verknotet werden.
Bei der Nahttechnik ist eine einreihige („single row“) von einer zweireihigen („double row“) Naht zu unterscheiden. Bei der einreihigen Naht wird der Anker in die Mitte des freiliegenden Anteils des Tuberculum majus eingedreht, bei der zweireihigen Naht wird ein Anker nahe an der Knorpelgrenze platziert und ein zweiter Anker außen am Tuberculum majus, um so einen flächigen Kontakt der Sehne mit dem Knochen zu erreichen (◘ Abb. 7.3). Sofern der Sehnenschaden groß ist, müssen mehrere Anker entlang dem Tuberculum majus eingebracht werden. Als Faustregel wird ein Ankerabstand von 1,5 cm empfohlen.
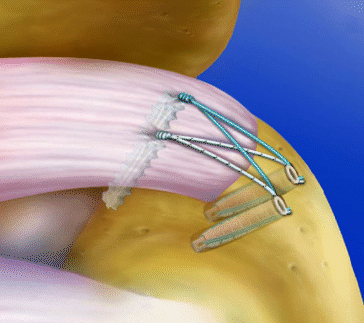
Abb. 7.3
Arthroskopische zweireihige Nahttechnik („double row repair“) (aus SutureBridge® Double Row Rotator Cuff Repair, Arthrex GmbH Karlsfeld 2010; mit freundl. Genehmigung)
Die Ankerfäden werden mit speziellen arthroskopischen Nahtzangen durch den Sehnenrand transportiert, die wie eine miniaturisierte Nähmaschine funktionieren (◘ Abb. 7.4). Alternativ können mit einer gebogenen kanülierten Nadel Hilfsfäden durch den Sehnenrand gestochen werden, mit deren Hilfe dann der eigentliche Ankerfaden eingezogen wird. Die transportierten Fäden werden von außen sortiert, vorgespannt und mithilfe eines arthroskopischen Knotenschiebers verknotet.
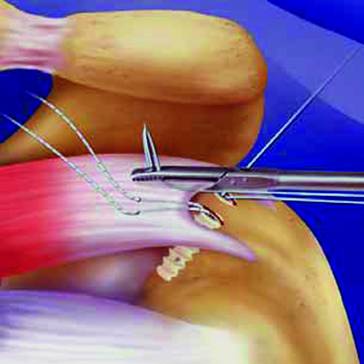
Abb. 7.4
Arthroskopische Nahtzange. (aus SutureBridge® Double Row Rotator Cuff Repair, Arthrex GmbH Karlsfeld 2010; mit freundl. Genehmigung)
Die arthroskopische Nahttechnik ist technisch schwierig und hat eine flache Lernkurve. Deshalb ist es zulässig, nach der subakromialen Dekompression in arthroskopischer Technik die eigentliche Sehnennaht offen auszuführen (sog. Mini Open-Technik). Hierzu erfolgt ein höchstens 5 cm langer Zugang, der vom AC-Gelenk ausgehend im Verlauf der Deltafasern angelegt wird. Der Ursprung des Deltamuskels wird auseinandergedrängt und kleine stumpfe Haken eingesetzt, um das Tuberculum majus darzustellen.
Die Sehnennaht erfolgt dann transossär mit nicht resorbierbaren Fäden, die durch den Sehnenrand gestochen werden. Den besten Halt erzielt ein U-förmiger Stich in sog. Mason-Allen-Technik. Die vorgelegten Fäden werden mit scharfen Nadeln oder einer Ahle durch den freiliegenden Anteil des Tuberculum majus transportiert und außen am Tuberculum majus verknotet. Die Ergebnisse dieser Mini Open-Technik unterscheiden sich langfristig nicht von den Ergebnissen der arthroskopischen Nähte.
Nachbehandlung
In den ersten 6 postoperativen Wochen hat der Sehnenansatz keine innere Festigkeit, weil er erst einheilen muss und die Sehne nur von den Nähten gehalten wird. In dieser Zeit besteht die Aufgabe der Physiotherapie darin, die Schmerzen zu vermindern und eine Einsteifung der Schulter durch passive Bewegungen zu verhindern. Auch hier sollte zunächst die Anteversion und danach die Abduktion geübt werden. Rotationsbewegungen sind besonders kritisch, weil sie die Naht stark belasten. Hier ist der Operateur gefragt, der die Festigkeit seiner Naht einschätzen und entsprechende Hinweise für die Behandlung geben muss. Bei großen Defekten mit entsprechend vielen Nahtankern bzw. Nähten wird die Nachsorge mehr Zurückhaltung benötigen als bei einem kleinen Defekt, der sich mit einem oder zwei Ankern verschließen lässt. Sofern nicht die Supraspinatussehne, sondern die Infraspinatus- oder die Subskapularissehne genäht wurde, sind die entsprechenden Bewegungsrichtungen mit besonderer Vorsicht zu beüben.
Abriss der langen Bizepssehne
OP-Indikation
Eine abgerissene lange Bizepssehne kann sich spontan im sanduhrförmigen Sulcus bicipitalis verklemmen, so dass keine weitere Therapie erforderlich ist. Andernfalls tritt der Muskelbauch sichtbar tiefer als auf der Gegenseite. Dies verursacht nur einen geringen Kraftverlust bei der Beugung des Ellenbogens und der Supination des Unterarms, der allenfalls Handwerker beeinträchtigt. Nicht selten sind die Symptome so gering, dass der Patient sie kaum bemerkt. Anfängliche Schmerzen bilden sich meistens innerhalb von 2 Wochen zurück. Eine echte Operationsindikation ergibt sich deshalb nur bei anhaltenden Krämpfen in dem verkürzten Muskel, die sehr unangenehm sein können, oder weil den Patienten die sichtbar veränderte Form des Muskels stört.
Operatives Vorgehen
Die abgerissene Sehne muss möglichst innerhalb von 6 Wochen im Sulcus bicipitalis refixiert werden. Verfahren mit einer hohen Primärstabilität sind die Schlüssellochtechnik oder die Befestigung in einem Bohrloch mit einer resorbierbaren Interferenzschraube, die auch in arthroskopischer Technik eingebracht werden kann.
Ursprungsläsionen der langen Bizepssehne
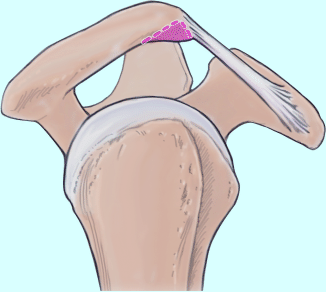
Ursprungsläsionen der langen Bizepssehne werden nach Snyder (Snyder et al. 1990) als SLAP-Läsionen (Superior Labrum from Anterior to Posterior) bezeichnet und in 4 Grundtypen eingeteilt (◘ Abb. 7.5). Bei seinen jüngeren Patienten, in einem Durchschnittsalter von 38 Jahren, fand sich zu 50 % eine traumatische Ursache. Ein typischer Mechanismus ist der Sturz auf die ausgestreckte Hand, der zu einer maximalen Einstauchung des Humeruskopfes unter das Schulterdach führt und den Bizepsanker stark beansprucht. Wesentlich häufiger sind degenerative SLAP-Läsionen bei älteren Patienten, die einer Zerfaserung des kranialen Labrums entsprechen und funktionell keine Bedeutung haben.
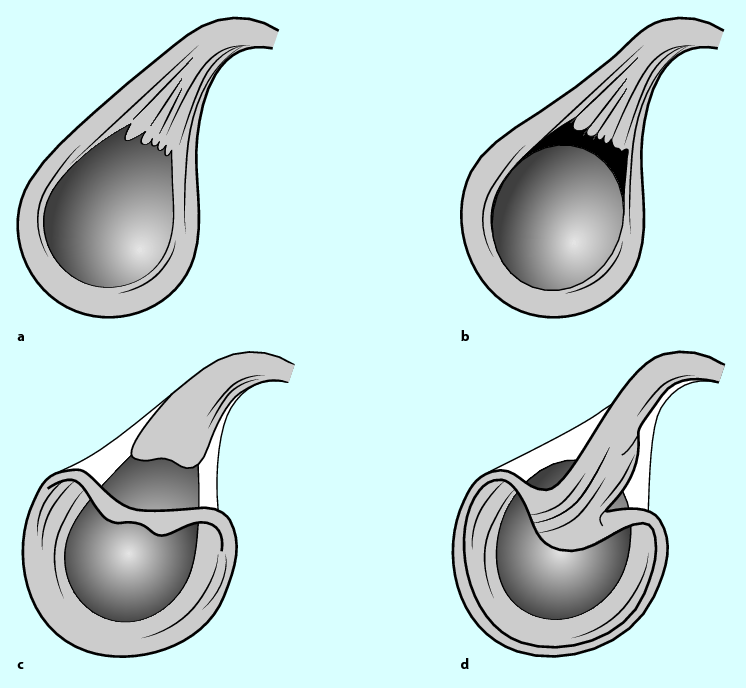
Abb. 7.5
Subtypen der SLAP-Läsionen nach Snyder (1990) Typ 1 zeigt vorwiegend eine Degeneration des Bizepssehnenankers (a), beim Typ 2 liegt eine instabile Ablosung vor (b). Beim Typ 3 finden wir eine korbhenkelartige Ablösung (c), die beim Typ 4 durch den Ursprung der langen Bizepssehne verläuft (d) (mod. nach Nebelung 2002)
Diagnosestellung
SLAP-Läsionen sind klinisch und kernspintomographisch nur schwer zu diagnostizieren. Sehr häufig handelt es sich deshalb um Zufallsbefunde bei einer Arthroskopie wegen anderer Beschwerden oder wegen unklarer Schmerzen.
Operatives Vorgehen
Das Labrum wird bis in seine stabilen Anteile zurückgeschnitten, sofern der Bizepsanker nicht betroffen ist (Typ 1 nach Snyder). Bei Typ 2, der den Bizepsursprung betrifft, und bei hochgradigen Schäden, die sich in die Bizepssehne hineinziehen (Typen 3 und 4), besteht die Therapie der Wahl darin, den abgerissenen Anteil des Labrums und den intraartikulären Anteil der langen Bizepssehne zu entfernen. Die Bizepssehne selbst wird dann im Sulkus tenodesiert. Ein Funktionsverlust für das Schultergelenk ist dabei nicht zu befürchten.
7.2.3 Traumatische Luxation
OP-Indikation
Die Wahrscheinlichkeit, nach einer primär-traumatischen Erstluxation einer gesunden Schulter ein Rezidiv zu entwickeln, ist umso höher, je jünger der Patient ist. Die Rezidivquote wird zudem durch sportliche Aktivität deutlich erhöht. Deshalb ist einem jungen Patienten bis zu 30 Jahren oder mit hohem sportlichen Anspruch schon nach der ersten traumatischen Luxation eine Stabilisierung der Schulter in arthroskopischer Technik zu empfehlen. Spätestens nach einem Rezidiv ergibt sich die eindeutige Indikation zum stabilisierenden Eingriff. Weitere Luxationen führen nur zu einer plastischen Deformierung der Kapsel und zu weiteren Schäden am Pfannenrand und am Humeruskopf. Auch rezidivierende Subluxationen stellen eine Operationsindikation dar!
Diagnosestellung
Die genaue Anamnese erlaubt es in vielen Fällen, zwischen einer traumatischen und einer atraumatischen Instabilitätsform zu unterscheiden (▶ Übersicht 7.1). Die klinische Untersuchung konzentriert sich auf die Überprüfung von Laxität und Stabilität der Schulter im Seitenvergleich (Einzelheiten zu den Tests ▶ Abschn. 7.2.7, Anhang):
Wie weit lässt sich der Humeruskopf gegenüber der Pfanne passiv verschieben?
Fällt der Apprehension-Test positiv aus?
Übersicht 7.1 Faktoren zur Einschätzung der Instabilitätsform
Faktoren, die für eine traumatische Instabilität sprechen:
Ausreichende Traumaschwere
Lange Zeitdauer bis zur Reposition
Reposition nur in Narkose möglich
Knöcherner Bankart-Defekt
Großer Hill-Sachs-Defekt
Faktoren, die für eine atraumatische (habituelle) Instabilität sprechen :
Kein adäquates Trauma
Laxität der Gegenschulter
Allgemeine Gelenklaxität
Willkürliche Luxationsneigung
Spontanreposition
Reposition durch einfachen Zug ohne Narkose
Kein Hill-Sachs-Defekt
Die folgenden bildgebenden Untersuchungen sollten vorliegen:
eine Standardröntgenserie in 3 Ebenen (true a.p., transskapulär, axial),
ein CT zur Beurteilung der knöchernen Situation an der Pfanne, sofern sich deren vordere Sklerosierungslinie in den Röntgenaufnahmen nicht einwandfrei darstellt, und
eine MRT zum Ausschluss eines zusätzlichen Schadens an der Rotatorenmanschette v. a. bei Patienten, die über 30 Jahre alt sind.
Operatives Vorgehen
Offene Stabilisierungsverfahren
Die vielen Operationsverfahren zur Behandlung der rezidivierenden, unidirektional vorderen Schulterinstabilität werden unterteilt in
anatomische Verfahren, welche die möglichst originalgetreue Rekonstruktion der zerstörten stabilisierenden Strukturen zum Ziel haben, und
nicht-anatomische Verfahren, die sekundäre Barrieren gegen die vermehrte Luxationsneigung des Humeruskopfes aufbauen.
Wegen der überlegenen Ergebnisse der anatomischen Verfahren sind diese zu bevorzugen.
Anatomische Verfahren
Bei der Operation nach Bankart (1939) wird der abgerissene Labrum-Kapsel-Komplex transossär am Pfannenrand refixiert (◘ Abb. 7.6). Das Ziel ist die Rekonstruktion der glenoidalen Kavität und des Ursprungs der glenohumeralen Bänder, besonders des inferioren glenohumeralen Bandes. Bei der vorderen Kapselplastik nach Neer (1990) wird die Kapsel plastisch rekonstruiert. Das Ziel ist die Normalisierung eines überweiteten Kapselvolumens und die Rekonstruktion der kompetenten glenohumeralen Bänder. Beide Verfahren werden kombiniert, wenn zu einer Bankart-Läsion ein überweitetes Kapselvolumen hinzutritt.
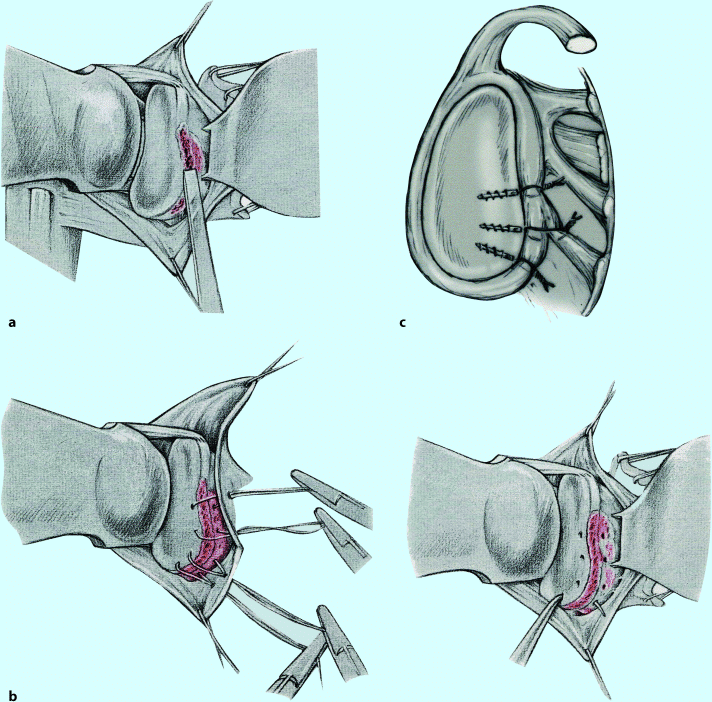
Abb. 7.6a–c
Bankart-Operation. a Der Pfannenrand wird angefrischt und b das Labrum mit transossären Nähten refixiert. c Bei der arthroskopischen Technik werden Knochenanker verwendet (aus Wiedemann 2010; mit freundl. Genehmigung)
Der Aufbau eines knöchern verbrauchten Pfannenrands mit einem J-Span in der Technik nach Resch (Maurer u. Resch 1995) hat zum Ziel, die knöcherne Kavität der Pfanne so anatomisch wie möglich wiederherzustellen. Die Rekonstruktion der Rotatorenmanschette, die bei einer vorderen Luxation abgerissen ist, erfolgt als transossäre Refixation am Tuberculum majus bzw. minus (s. oben).
Technik der Operation nach Bankart
Der Patient wird halbsitzend gelagert. Mit einem kurzen sagittalen Zugang wird der Sulcus deltoideopectoralis eröffnet. Der M. subscapularis wird 1 cm medial des Tuberculum minus durchtrennt und nach medial von der Kapsel abgelöst, die T-förmig eröffnet wird. Der knöcherne Pfannenrand wird angefrischt (◘ Abb. 7.6) und mehrere quere Löcher angelegt, die zur knöchernen Reinsertion des Labrums und des abgerissenen Kapselursprungs dienen. Alternativ können resorbierbare Knochenanker verwendet werden. Nach dem Verschluss der Kapsel wird der M. subscapularis ohne Verkürzung refixiert.
Technik der Kapselplastik nach Neer
Findet sich trotz eindeutiger unidirektional vorderer Instabilität intraoperativ keine Bankart-Läsion, muss zunächst den wirklichen Ursachen der Luxationsneigung nachgegangen werden. In Betracht kommen knöcherne Defekte und ein nicht erkannter Abriss der Kapsel vom Humeruskopf (sog. HAGL-Läsion). Bei einer Kapselinsuffizienz muss diese behandelt werden. Der Zugang erfolgt wie bei der Bankart-Operation. Das nach der T-förmigen Inzision entstehende untere Kapseldreieck wird nach kranial gezogen und am Tuberculum minus refixiert. Anschließend wird das kraniale Kapseldreieck nach kaudal gezogen und ebenfalls am Tuberculum minus refixiert. Der Arm wird dabei in 30° Abduktion und 30° Außenrotation gelagert. Durch die Doppelung entstehen neue, besonders kräftige glenohumerale Bänder.
J-Span nach Resch
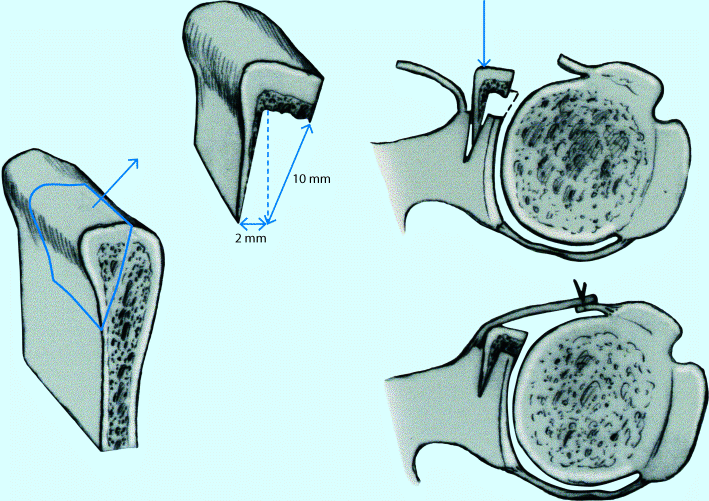
Im Fall eines ausgeprägten knöchernen Pfannenranddefekts ist eine Bankart-Operation nicht sinnvoll, weil bei einer zu kleinen Pfanne deren Kavität nicht wiederhergestellt werden kann. Dann ist ein Pfannenaufbau mit einem J-Span angezeigt (◘ Abb. 7.7). Hierzu wird vom Beckenkamm ein bikortikaler Span gehoben, dessen spongiöse Innenseite so geformt wird, dass der Span im Profil J-förmig erscheint. Am Skapulahals wird ein knöcherner Schlitz vorbereitet, in den der Span eingebolzt wird. Mit einer kleinen Fräse wird der Span exakt dem Niveau der Gelenkfläche angepasst, um einen möglichst glatten Übergang zu erzielen.
Nicht-anatomische Verfahren
Der Korakoidtransfer in der Modifikation von Patte (Patte et al. 1980) funktioniert auch bei einem knöchernen Verbrauch der Pfanne. Die Methode sieht 3 Schritte vor („triple verrouillage“):
das Versetzen der Korakoidspitze an den ventralen Skapulahals,
die Verstärkung der Kapsel durch einen Teil des korakoakromialen Bandes und
den Erhalt des M. subscapularis.
Ziele sind die Rekonstruktion der Kapsel und die Bildung einer muskulären „Hängematte“ durch die versetzten kurzen Oberarmbeuger.
Alle anderen nicht-anatomischen Verfahren einschließlich der Rotationsosteotomie nach Weber sind wegen ihrer Nachteile und der höheren Gefahr einer Sekundärarthrose nicht mehr gebräuchlich. Der Korakoidtransfer wird in Frankreich als Standardverfahren zur Stabilisierung der Schulter verwendet und wird deshalb auch hier zunehmend populär. Dennoch werden gegenwärtig in Deutschland mehr als 90 % der Schultern mit einem anatomischen Verfahren stabilisiert.
Arthroskopische Stabilisierungsverfahren
Die Rekonstruktion des vorderen Pfannenrands nach Bankart kann auch arthroskopisch erfolgen. Dies hat den Vorteil, dass der M. subscapularis nicht durchtrennt werden muss. Allerdings hat sich gezeigt, dass die Rezidivquote nach dem arthroskopischen Vorgehen höher sein kann als beim offenen Verfahren. Entscheidend für ein stabiles Ergebnis ist hier die Frage, ob der Pfannenrand knöchern intakt ist. Dies muss vor einem arthroskopischen Eingriff in einer MRT oder einem CT gesichert werden.
Stay updated, free articles. Join our Telegram channel

Full access? Get Clinical Tree