Résumé
La négligence spatiale (NS) constitue un facteur de mauvais pronostic fonctionnel. L’adaptation à une déviation prismatique de la vision vers la droite améliore la NS. Les bases neurophysiologiques et les modalités optimales de l’adaptation prismatique (AP) restent à valider. Cette étude vise à explorer les effets sensori-moteurs, cognitifs et fonctionnels à long terme produits par une séance d’AP hebdomadaire pendant 4 semaines. Un essai monocentrique, en double insu, randomisé et contrôlé a été réalisé. Vingt patients avec NS gauche secondaire à un accident vasculaire cérébral droit ont été inclus (10 dans le groupe « prisme » et 10 dans le groupe « témoin »). Les effets sensori-moteurs de l’AP ont été évalués par des mesures des droit-devant manuel et visuel, et par la précision du pointage sans rétroaction visuelle avant et après chaque séance d’AP. La mesure de l’indépendance fonctionnelle (MIF) était évaluée avant et 1, 3 et 6 mois après AP, la sévérité de la NS par l’échelle Behavioural Inattention Test (BIT) avant et 6 mois après AP. Au terme des 6 mois de suivi, les deux groupes montraient une amélioration similaire, corrélée à l’évolution du droit-devant visuel, marqueur de l’évolution des patients. Une séance d’AP hebdomadaire pendant 4 semaines s’avère une posologie insuffisante pour produire un bénéfice fonctionnel à long terme. Avant intervention, seul le droit-devant manuel constituait une mesure sensori-motrice reproductible. Pendant l’exposition prismatique, un questionnaire a montré qu’aucun patient n’a perçu les effets directs de la déviation optique sur le déroulement du geste de pointage. Les effets consécutifs sensori-moteurs produits par ce régime d’AP ont favorisé la réduction plus rapide du droit-devant manuel vers la gauche, suivie secondairement par le droit-devant visuel, ce qui permet d’éclairer les mécanismes d’action de l’AP sur la NS.
1
Introduction
La négligence spatiale (NS) se définit comme une difficulté singulière à détecter, répondre ou orienter son attention vers des stimuli présentés ou représentés du côté controlatéral à une lésion cérébrale, en particulier de l’hémisphère droit . Ce syndrome majore la sévérité des déficits moteurs et sensoriels associés et constitue un facteur de mauvais pronostic fonctionnel . Plusieurs méthodes de rééducation ont été proposées pour réduire le biais comportemental dirigé du côté de la lésion cérébrale et le défaut de conscience de l’hémi-espace controlatéral de la NS avec un faible niveau de preuve . À partir d’une méta-analyse ayant inclus 23 essais cliniques randomisés (628 participants), Bowen et al. ont montré que la plupart des études évaluent l’effet des rééducations sur des tests standardisées d’évaluation ; 15 études ont évalué l’impact sur les activités de la vie quotidienne immédiatement après la rééducation et seulement 6 études ont mesuré ces effets à distance. Les résultats disponibles actuellement montrent un effet significatif en faveur des rééducations cognitives, mais seulement sur les tests d’évaluation standardisée de la NS. L’efficacité sur les activités de la vie quotidienne n’est donc pas rigoureusement démontrée.
Parmi ces méthodes, la rééducation par adaptation prismatique (AP) est l’une des méthode qui apparaît comme la plus utilisée et efficace à court terme . Ses effets recouvrent un très large panel de fonctions perceptives, cognitives ou motrices affectées dans la NS : la négligence visuelle , la négligence somatosensorielle et haptique , l’extinction tactile , l’extinction auditive , la négligence représentationnelle , des représentations numériques ainsi que l’écriture , ou le déplacement en fauteuil roulant . Des bénéfices ont également été observés sur le déséquilibre postural chez des patients après rémission clinique de leur NS .
Les effets de l’AP sont étonnement prolongés dans le temps par rapport aux durées connues chez le sujet sain. Depuis notre étude initiale qui rapportait des effets durant au moins deux heures à la suite de quelques minutes d’exercice visuo-moteur sous prismes , des effets prolongés ont été rapportés après une seule séance d’AP sur la négligence visuelle , ainsi que sur des manifestations cliniques comme la lecture , l’écriture et la déambulation en fauteuil roulant . De façon plus pertinente pour la rééducation, la durée des effets obtenus est prolongée après des séances répétées d’adaptation. Plusieurs études non randomisées et randomisées ont rapporté des effets à long terme, supérieurs à 5 semaines, à la suite d’une rééducation intensive comprenant deux séances d’AP par jour pendant 2 semaines. Dans un essai randomisé contrôlé ayant inclus 38 patients avec NS (20 rééduqués et 18 témoins), un bénéfice fonctionnel lié à l’AP a été observé à la sortie de l’hôpital seulement dans le sous-groupe de patients avec NS modérée .
Pour mettre au point un protocole de rééducation, il est nécessaire de cerner la durée des effets d’une séance isolée d’AP. L’amélioration cognitive rapportée après une seule séance est généralement maximale 24 heures après l’AP, puis persiste avec une durée de l’ordre de quelques jours à une semaine . Compte tenu de l’amoindrissement des effets consécutifs avec la répétition des séances d’adaptation, nous avons choisi d’espacer les séances d’AP. Prenant également en compte le fait que les effets sensori-moteurs de l’AP présentent une durée de plusieurs jours , nous avons décidé de tester un régime composé d’une séance d’AP par semaine. En contrepartie, nous avons prolongé la durée de rééducation à un mois au lieu des périodes de deux semaines utilisées dans la plupart des essais thérapeutiques . Le but principal de cet essai contrôlé randomisé en double insu est donc d’explorer les effets d’une posologie modérée d’AP consistant en une séance d’AP hebdomadaire pendant 4 semaines sur la NS et les activités de la vie quotidienne chez des patients chroniques. L’intérêt clinique potentiel de ce régime d’adaptation prismatique allégé serait de permettre une prise en charge thérapeutique en ambulatoire.
Le second objectif de cette étude est de suivre l’évolution des référentiels spatiaux au cours de la récupération des patients négligents et de clarifier la relation existant entre les effets consécutifs sensori-moteurs de l’AP et l’expansion de ces effets à la sphère cognitive . En effet, des dissociations entre ces deux niveaux d’action de l’AP ont été rapportées alors que certaines études ont observé une corrélation significative entre les effets consécutifs proprioceptifs et la NS . L’existence ou non d’un lien quantitatif entre les conséquences sensori-motrices et cognitives de l’AP dans la NS est fondamentale pour la conception et la validation d’études pilotes réalisées chez le sujet sain, mais aussi afin de disposer de facteurs pronostiques objectifs et immédiats du bénéfice thérapeutique attendu chez un patient donné. Cette étude inclut donc la mesure de paramètres sensori-moteurs permettant à la fois de suivre l’évolution des référentiels spatiaux des patients et de quantifier l’AP : le droit-devant manuel (DDM), le droit-devant visuel (DDV) et le pointage sans rétroaction visuelle (ou en boucle ouverte ; PSRV). Compte tenu de la confusion existant chez certains auteurs entre adaptation visuo-motrice et réduction des erreurs pendant l’exposition à une déviation, conduisant à la conclusion erronée que l’adaptation est déficiente chez les patients négligents , l’exploration détaillée de ces paramètres vise également à clarifier comment mesurer l’adaptation prismatique vraie . La question de l’altération ou de la facilitation du processus d’adaptation dans la négligence est de plus abordée par un questionnaire évaluant la conscience des patients pour la déviation prismatique. La fiabilité et la valeur prédictive de ces variables, encore non décrites dans la littérature, sont également explorées dans cette étude.
2
Méthodes
2.1
Patients
Dix-neuf patients admis dans le service de médecine physique et réadaptation neurologique, hôpital Henry-Gabrielle, hospices civils de Lyon et présentant une NS gauche secondaire à un accident vasculaire droit ont été inclus dans l’étude de septembre 2001 à septembre 2005 ( Fig. 1 ). Tous les patients étaient droitiers selon le questionnaire d’Edimburgh .
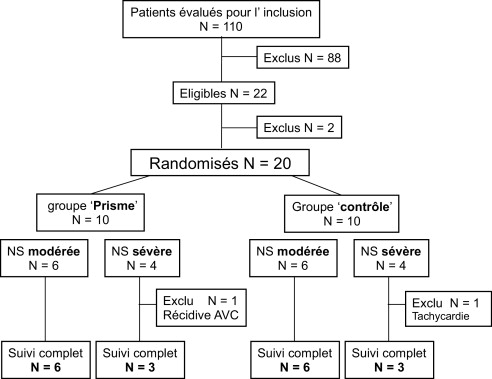
Les critères d’inclusion étaient :
- •
un âge compris entre 18 et 90 ans ;
- •
un accident vasculaire cérébral unique confirmé par un examen tomodensitométrique ou d’imagerie par résonance magnétique cérébrale ;
- •
une NS gauche confirmée par les tests neuropsychologiques suivants (test de bissection de lignes , test des ballons , copie de dessin, dictée d’un texte et lecture d’un texte) ;
- •
un délai d’au moins un mois après la survenue de l’ictus.
Les critères d’exclusion étaient :
- •
l’existence de lésions cérébrales multiples ;
- •
une désorientation temporo-spatiale ;
- •
des troubles psychiatriques ;
- •
une pathologie associée non stabilisée.
Les caractéristiques des patients des deux groupes sont détaillées dans le Tableau 1 .
| Cas | NS | Âge / sexe | IL | DM | DS | HLH G | DTY | Délai | Étiologie | Lésion |
|---|---|---|---|---|---|---|---|---|---|---|
| Groupe prisme | ||||||||||
| 1 | N+ | 40 / F | 100 | 3 | 3 | P | 1 | 44 | Isch | Frontal, parietal, occipital, temporal, insula, corona radiata, putamen |
| 7 | N | 40 / F | 100 | 3 | 3 | P | 2 | 47 | Isch | Frontal, parietal, temporal, insula, corona radiata, putamen |
| 8 | N | 47 / F | 100 | 3 | 0 | P | 1 | 34 | Isch | Corona radiata, substance blanche frontale), insula, capsule interne, putamen, noyau caudé |
| 9 | N | 69 / M | 100 | 3 | 3 | P | 0 | 54 | Isch | temporal (occipital), corona radiata, capsule interne, putamen |
| 10 | N | 66 / M | 16,66 | 3 | 3 | A | 2 | 60 | Isch | Frontal, parietal (temporal), corona radiata, putamen |
| 11 | N | 59 / M | 100 | 2 | 2 | P | 1 | 88 | Hem | Parietal, occipital |
| 13 | N | 49 / M | 100 | 3 | 3 | P | 1 | 30 | Isch | Frontal (temporal, parietal), putamen |
| 15 | N | 63 / F | 100 | 3 | 3 | P | 1 | 42 | Isch | Corona radiata, capsule interne, putamen |
| 16 | N | 71 / M | 100 | 3 | 3 | P | 1 | 60 | Isch | Frontal, parietal, corona radiata, putamen |
| Groupe témoin | ||||||||||
| 2 | N | 45 / M | 83,33 | 3 | 3 | A | 1 | 35 | Isch | Corona radiata, substance blanche frontale, insula, capsule interne, putamen |
| 3 | N | 45 / M | 100 | 3 | 3 | A | 1 | 92 | Isch | Substance blanche frontale, corona radiata, insula, putamen, noyau caudé |
| 4 | N | 57 / M | 100 | 3 | 3 | P | 1 | 38 | Isch | Frontal, temporal, parietal, insula, putamen |
| 5 | N | 72 / M | 100 | 3 | 3 | A | 1 | 60 | hem | Corona radiata, insula, capsule interne, putamen |
| 6 | N | 62 / F | 91,66 | 3 | 3 | P | 1 | 46 | Isch | Parietal, occipital |
| 12 | N | 79 / F | 100 | 2 | 2 | P | 1 | 38 | Hem | Parietal, occipital |
| 14 | N | 51 / M | 100 | 3 | 3 | P | 2 | 67 | Isch | Temporal, parietal, occipital |
| 17 | N | 75 / F | 100 | 1 | 1 | P | 1 | 34 | Isch | Occipital, substance blanche pariétale, putamen, noyau caudé |
| 18 | N | 69 / F | 100 | 3 | 2 | P | 2 | 60 | Isch | Frontal, temporal, parietal, corona radiata, putamen, noyau caudé |
2.2
Description de l’étude
Il s’agit d’un essai clinique randomisé contrôlé monocentrique en double insu comprenant 2 groupes de patients présentant une NS gauche : un groupe bénéficiant de la rééducation par AP et un groupe témoin. Le critère de jugement principal de l’étude était l’amélioration fonctionnelle dans les actes de la vie quotidienne après rééducation et mesurée par la mesure de l’indépendance fonctionnelle (MIF) . Ce score a été utilisé dans un essai clinique non randomisé évaluant l’efficacité d’une orthèse de tronc dans la rééducation de la NS chez deux groupes de patients . Ces auteurs ont montré, à 6 mois d’évolution, une différence statistiquement significative entre les scores moyens des 2 groupes (différence moyenne = 24 ; n = 11). Sachant que dans cette étude précédente, le critère de jugement MIF avait un écart-type de 10 unités, pour avoir 90 chances sur 100 au moins de mettre en évidence une différence de 25 points entre les réponses moyennes des deux groupes (avec un risque d’erreur de première espèce au plus égal à 5 %), il faudra inclure au minimum 9 sujets par groupe (c’est-à-dire : 1–β = 0,90 ; β = 0,10 ; α = 0,05 et Δ = 25 ; n = σ 2 × M/ Δ 2 = 100 × 54/625 = 8,6, soit au moins 9 sujets).
Une randomisation par bloc a été réalisée avec une distinction de deux niveaux de sévérité du déficit selon la gravité initiale de la NS évaluée par les tests d’inclusion : NS sévère : déficit présent à tous les tests d’inclusion, score au test de Schenkenberg et al. supérieur à 50 % de déviation et score de BIT ≤ 55 ; NS modérée : déficit présent à certains tests d’inclusion (de 1 à 4), score au test de Shenkenberg et al. compris entre 11 et 50 % de déviation et score de BIT > 55.
Il s’agit d’une étude en double insu : les examinateurs réalisant l’évaluation (G.R., S.L., E.M.) ignoraient si le patient inclus a bénéficié d’une AP ou non. Ils étaient distincts des examinateurs réalisant la tâche d’exposition aux lunettes prismatiques ou aux verres neutres (Y.R., S.J.C., L.P.). Par ailleurs, la procédure en double insu a été facilitée par le fait que les patients avec NS ne sont pas conscients de la perturbation induite par la déviation prismatique et ne présentent pas les réactions végétatives attendues lors de l’apparition d’erreurs motrices au début du port de prismes (cf. infra et ), ce qui permet de les affecter au groupes « prisme » et « témoin » à leur insu. De plus, cela permet aux investigateurs réalisant les évaluations de ne pas recevoir d’informations de la part des patients, qui pourraient dégrader le double insu en simple insu.
La randomisation par bloc et le tirage au sort répartissant les patients dans le groupe « prisme » ou « témoin » ont été réalisés par monsieur Denis Pélisson, directeur de l’équipe ImpAct, du centre de recherche en neurosciences de Lyon. Une randomisation à 2 niveaux a été réalisée : à un premier niveau, par la sélection des patients dans le groupe « prisme » ou « témoin », puis à un 2 e niveau, par la sélection des patients selon la gravité de la NS initiale à partir du score BIT, afin que le ratio patients atteints d’une négligence sévère et patients atteints d’une négligence modérée soit comparable dans les deux groupes.
Tous les patients ont donné leur consentement pour la participation à cette étude. La procédure expérimentale a été approuvée par le Comité consultatif de protection des personnes dans la recherche biomédicale Lyon B le 5 juin 2001 (dossier 2001-040 B). Les hospices civils de Lyon ont été le promoteur de cette étude, enregistrée le 2 août 2001 sous le numéro 2001/0294 . Le financement de l’étude a été assuré par l’ Inserm , les hospices civils de Lyon et l’ université Claude-Bernard – Lyon-1 .
2.3
Paramètres de l’étude
Les référentiels spatiaux et la précision des pointages vers une cible visuelle (réalisés sans rétroaction visuelle) ont été mesurés de l’inclusion du patient jusqu’à six mois afin de suivre leur évolution au cours de la récupération des patients. Une double mesure a de plus été réalisée, avant et après chaque séance d’exposition, afin de quantifier les effets consécutifs de l’adaptation prismatique.
Le critère de jugement d’efficacité thérapeutique principal est le score fonctionnel obtenu à partir de l’échelle de mesure de l’indépendance fonctionnelle (MIF) . Le critère secondaire est le score total du Behavioural Inattention Test (BIT) , reflétant la sévérité de la NS. La mesure du critère de jugement principal a été réalisée à 4 reprises : en pré-test et en post-tests à 1 (M1), 3 (M3) et 6 mois (M6) après la première séance d’AP. Pour la batterie BIT, deux évaluations ont été réalisées en pré-test et en post-tests à 6 mois ; aucune évaluation intermédiaire n’a été réalisée en cours de suivi afin de limiter l’effet confondant d’un apprentissage lié à la répétition des tests.
2.4
Adaptation prismatique et paramètres sensori-moteurs
Dans le groupe « prisme », l’AP a été obtenue par le port d’une paire de lunettes produisant une déviation optique du champ visuel de 10° vers la droite (OptiquePeter.com). Les verres prismatiques étaient composés de deux verres courbes point par point de 5° chacun, ajustés à une monture glacier avec des œillères latérales, afin d’éviter l’accès à la vision non décalée. Ces prismes couvraient un champ visuel total de 105° dont chaque champ monoculaire représentait 75° et le champ visuel binoculaire central 45°.
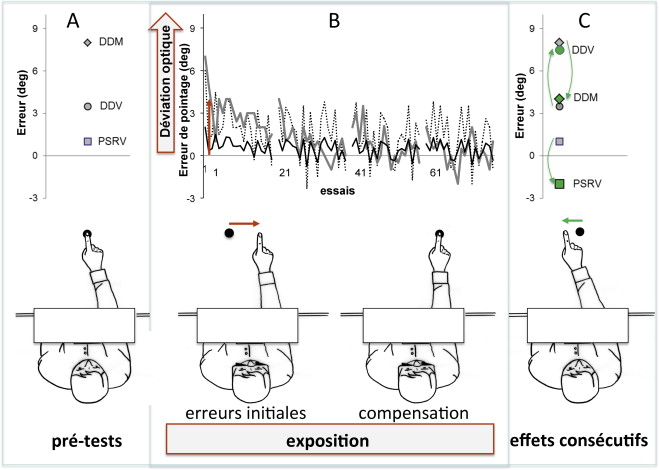
Pendant l’exposition prismatique, le patient devait réaliser 80 mouvements de pointage rapides en direction de cibles visuelles situées à 10 degrés à droite ou à gauche par rapport au milieu de son corps, alternées de façon pseudo-aléatoire. En dépit de l’instruction répétée de réaliser des mouvements rapides, la vitesse de mouvement des patients cérébrolésés reste généralement assez lente pour autoriser une rétroaction visuelle et les erreurs produites ne reflétaient pas toujours l’amplitude de la déviation optique ou le stade de l’adaptation ( Fig. 2 ). Cette vitesse restait cependant compatible avec le développement d’une adaptation sensori-motrice vraie en limitant les composantes stratégiques de la compensation . Les mouvements de pointage étaient réalisés avec une pause d’environ 30 secondes après chaque série de 20 permettant de favoriser une augmentation des erreurs au début de la série suivante. Durant l’exposition, le patient ne voyait pas la position initiale de la main, qui entrait dans le champ visuel entre le tiers et la moitié de son mouvement , afin de favoriser un codage proprioceptivo-visuel du mouvement . La durée de l’exposition prismatique était comprise entre 6 et 10 minutes. Les patients du groupe « témoin » réalisaient cette tâche visuo-motrice dans les mêmes conditions mais avec le port d’une paire de lunettes placebo, équipée de verres neutres de même poids et composées de deux verres prismatiques de 5 degrés collés en opposition et ne produisant aucune déviation optique ( ; OptiquePeter.com). Chaque patient a effectué la tâche d’exposition (avec lunettes prismatiques ou verres neutres) à 4 reprises : à j0 (Expo1), à j + 7 (Expo2), à j + 14 (Expo3) et à j + 21 (Expo4). Toutes les séances d’exposition ont été réalisées dans les mêmes conditions et avec les mêmes opérateurs.
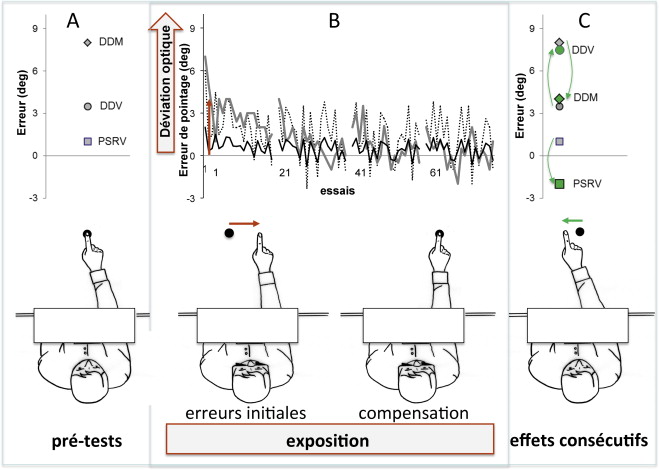
La conscience perceptive des patients pour la déviation optique et ses conséquences sur le déroulement du geste ont été étudiées systématiquement par un questionnaire phénoménologique ( Annexe 1 ). Ce questionnaire ouvert comprend 20 questions regroupées en 3 grandes parties, et évoluant de formulations très ouvertes jusqu’à des questions très spécifiques sur la déviation prismatique. La première partie comprend 5 questions très ouvertes posées après une dizaine de pointages préliminaires réalisés avant de chausser les lunettes. Ces questions progressent de (Q1 : comment se passe l’exercice ?) et (Q3 : avez-vous observé quelque chose de particulier ?) jusqu’à (Q5 : est-ce que c’est facile de viser vers la cible ?). La deuxième partie, principale, est administrée après 5 mouvements réalisés avec les lunettes, donc pendant la période précoce de l’exposition qui génère habituellement les erreurs maximales de pointage . Cette deuxième partie de 12 questions reprend initialement les 5 questions ouvertes précédentes (Q6 à Q10), puis propose des questions de plus en plus explicites (Q11 à Q17 ; Q17 : chez certains patients, ces lunettes peuvent entraîner des difficultés pour viser avec la main. Comment cela se passe-t-il pour vous ?). La troisième partie du questionnaire (Q18 à Q20) est proposée après 20 mouvements et à la fin de la période d’adaptation.
Les effets consécutifs de l’AP ont été évalués par des mesures répétées du DDM dans l’obscurité ( n = 10), du DDV dans l’obscurité ( n = 10) et du PSRV vers une cible visuelle ( n = 10). Les DDV et DDM présentent un double intérêt dans le cadre de cette étude car ils sont classiquement utilisés de façon indépendante pour évaluer la référence égocentrique , et par soustraction des mesures obtenues avant et après exposition aux prismes (VS : visual shift et PS : proprioceptive shift ), pour quantifier les effets consécutifs de l’AP . Le PSRV est utilisé pour mesurer par la même soustraction (TS : total shift ) les effets consécutifs totaux de l’AP . Ces trois paramètres sensori-moteurs ont été évalués en pré-test, en post-tests à 1 (M1), 3 (M3) et 6 mois (M6) pour suivre l’évolution des référentiels de chaque patient, ainsi qu’avant et après chaque séance d’exposition prismatique (Expo1, Expo2, Expo3 et Expo4) dans le but de quantifier l’adaptation. Afin d’éviter de contaminer les mesures sensori-motrices par des paramètres cognitifs pouvant être impliqués dans la compensation de la déviation prismatique indépendamment de l’adaptation , un soin tout particulier a été porté sur l’utilisation de conditions différentes pendant les évaluations des pré- et post-tests et pendant l’exposition aux prismes : la cible utilisée pour le PSRV et les consignes de précision/vitesse étaient différentes de celles utilisées pendant l’exposition.
La mesure du DDM a été réalisée en demandant au patient de pointer avec sa main droite dans l’obscurité en position « droit-devant dans la direction d’une ligne imaginaire séparant leur corps en deux moitiés équivalentes ». Le sujet déployait son bras sans contrainte de vitesse ou d’amplitude, et l’on lui rappelait si nécessaire qu’il n’était pas attendu qu’il aille vite ou étire le bras au maximum. La mesure du pointage était effectuée à l’aide d’un contacteur soudé sur un dé à coudre enfilé sur l’index droit, au-dessus d’une table recouverte d’un papier carbone isorésistif, sur laquelle étaient appliquées deux électrodes de 65 × 1 cm définissant ainsi un secteur d’angle de 50° centré sur la position de départ près du torse, et d’une profondeur de 70 cm. Entre les électrodes, était généré un courant continu de 5 V. Lorsque le doigt atteignait la surface de la table, la tension était mesurée entre le contact du dé et l’électrode de référence comme dans un potentiomètre. Cette tension permettait de calculer la position angulaire par rapport à l’axe sagittal objectif, convertie en degrés et signée conventionnellement (négatif à gauche et positif à droite ; Fig. 3 A ). La précision de cette mesure est estimée à ±0,5 degrés.

La mesure du DDV a été réalisée dans l’obscurité totale. Le patient était assis confortablement devant une table, la tête était maintenue droite par une mentonnière . Une diode luminescente rouge était déplacée par l’expérimentateur sur une rampe horizontale de deux mètres fixée à une distance d’un mètre en face du patient. La vitesse de déplacement était comprise entre 20 et 30 cm/s. Dix mesures successives étaient réalisées en alternant le déplacement de la cible dans le sens droite-gauche et dans le sens opposé. On demandait au patient d’interrompre verbalement (« stop ! ») le déplacement de la cible lorsqu’il la percevait en position « droit-devant » ( Fig. 3 B). La mesure de la déviation était réalisée grâce à un galvanomètre calibré et convertie en déviation angulaire par rapport au droit-devant objectif.
La mesure du PSRV a été réalisée dans les mêmes conditions d’obscurité et avec le même dispositif ( Fig. 3 C). La cible visuelle lumineuse était alignée avec l’axe sagittal du patient. L’instruction donnée au patient pour ce test était de placer sa main droite à l’aplomb de la cible, en privilégiant la précision et sans aucune contrainte de temps, afin de s’éloigner des conditions de pointage utilisées pendant l’exposition et d’obtenir une mesure des effets consécutifs sensori-moteurs moins polluée par des facteurs cognitifs .
Au cours de l’exposition prismatique, les erreurs terminales de chaque mouvement étaient relevées au moyen du dé à coudre et converties en degrés d’erreur angulaire par rapport à la cible visée.
2.5
Analyse statistique
Les résultats des deux groupes aux pré-tests ont d’abord été comparés. Une première analyse de variance à mesures répétées a comparé les deux groupes pour les paramètres suivants (âge, MIF, BIT, délai moyen post-AVC). Les paramètres sensori-moteurs ont été comparés par une rmANOVA (analyse de variance à mesures répétées) incluant le facteur session puisque deux pré-tests étaient disponibles. La fiabilité de ces mesures sensori-motrices a été évaluée par une corrélation.
L’évaluation des effets sensori-moteurs a procédé en deux étapes principales. Les premiers tests ont comparé les différences effets consécutifs mesurés par la différence post-pré par des tests- t de Student unilatéral contre la valeur théorique zéro. Une analyse de variance à mesures répétées à trois facteurs a ensuite comparé les deux traitements (facteur groupe, inter-sujet : prisme et témoin) avec deux facteurs intra-sujets : pré-post (mesure avant et après exposition) et session (Expo1 à Expo4). Les courbes de réduction d’erreurs obtenues pendant l’exposition n’étaient pas interprétables du fait de la vitesse de mouvement à la fois variable et lente des patients.
Afin d’étudier l’impact à long terme des 4 séances d’AP sur les variables sensori-motrices, une analyse de variance à mesures répétées a été réalisée avec les facteurs « session » (pré, M1, M3, M6 ou pré et M6), « groupe » (prisme, témoin) pour chaque paramètre fonctionnel étudié.
Pour terminer, les résultats ont également permis d’explorer la valeur prédictive des paramètres sensori-moteurs sur les scores BIT et MIF, ainsi que sur leur évolution entre les pré-tests et M6.
2
Méthodes
2.1
Patients
Dix-neuf patients admis dans le service de médecine physique et réadaptation neurologique, hôpital Henry-Gabrielle, hospices civils de Lyon et présentant une NS gauche secondaire à un accident vasculaire droit ont été inclus dans l’étude de septembre 2001 à septembre 2005 ( Fig. 1 ). Tous les patients étaient droitiers selon le questionnaire d’Edimburgh .
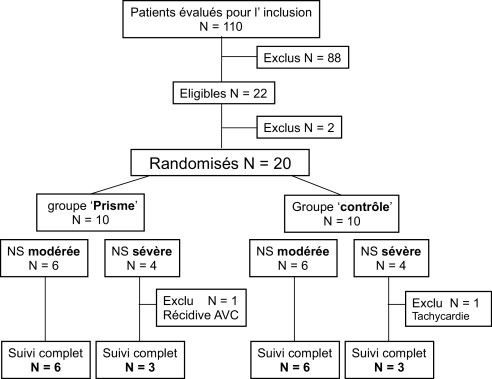
Les critères d’inclusion étaient :
- •
un âge compris entre 18 et 90 ans ;
- •
un accident vasculaire cérébral unique confirmé par un examen tomodensitométrique ou d’imagerie par résonance magnétique cérébrale ;
- •
une NS gauche confirmée par les tests neuropsychologiques suivants (test de bissection de lignes , test des ballons , copie de dessin, dictée d’un texte et lecture d’un texte) ;
- •
un délai d’au moins un mois après la survenue de l’ictus.
Les critères d’exclusion étaient :
- •
l’existence de lésions cérébrales multiples ;
- •
une désorientation temporo-spatiale ;
- •
des troubles psychiatriques ;
- •
une pathologie associée non stabilisée.
Les caractéristiques des patients des deux groupes sont détaillées dans le Tableau 1 .
| Cas | NS | Âge / sexe | IL | DM | DS | HLH G | DTY | Délai | Étiologie | Lésion |
|---|---|---|---|---|---|---|---|---|---|---|
| Groupe prisme | ||||||||||
| 1 | N+ | 40 / F | 100 | 3 | 3 | P | 1 | 44 | Isch | Frontal, parietal, occipital, temporal, insula, corona radiata, putamen |
| 7 | N | 40 / F | 100 | 3 | 3 | P | 2 | 47 | Isch | Frontal, parietal, temporal, insula, corona radiata, putamen |
| 8 | N | 47 / F | 100 | 3 | 0 | P | 1 | 34 | Isch | Corona radiata, substance blanche frontale), insula, capsule interne, putamen, noyau caudé |
| 9 | N | 69 / M | 100 | 3 | 3 | P | 0 | 54 | Isch | temporal (occipital), corona radiata, capsule interne, putamen |
| 10 | N | 66 / M | 16,66 | 3 | 3 | A | 2 | 60 | Isch | Frontal, parietal (temporal), corona radiata, putamen |
| 11 | N | 59 / M | 100 | 2 | 2 | P | 1 | 88 | Hem | Parietal, occipital |
| 13 | N | 49 / M | 100 | 3 | 3 | P | 1 | 30 | Isch | Frontal (temporal, parietal), putamen |
| 15 | N | 63 / F | 100 | 3 | 3 | P | 1 | 42 | Isch | Corona radiata, capsule interne, putamen |
| 16 | N | 71 / M | 100 | 3 | 3 | P | 1 | 60 | Isch | Frontal, parietal, corona radiata, putamen |
| Groupe témoin | ||||||||||
| 2 | N | 45 / M | 83,33 | 3 | 3 | A | 1 | 35 | Isch | Corona radiata, substance blanche frontale, insula, capsule interne, putamen |
| 3 | N | 45 / M | 100 | 3 | 3 | A | 1 | 92 | Isch | Substance blanche frontale, corona radiata, insula, putamen, noyau caudé |
| 4 | N | 57 / M | 100 | 3 | 3 | P | 1 | 38 | Isch | Frontal, temporal, parietal, insula, putamen |
| 5 | N | 72 / M | 100 | 3 | 3 | A | 1 | 60 | hem | Corona radiata, insula, capsule interne, putamen |
| 6 | N | 62 / F | 91,66 | 3 | 3 | P | 1 | 46 | Isch | Parietal, occipital |
| 12 | N | 79 / F | 100 | 2 | 2 | P | 1 | 38 | Hem | Parietal, occipital |
| 14 | N | 51 / M | 100 | 3 | 3 | P | 2 | 67 | Isch | Temporal, parietal, occipital |
| 17 | N | 75 / F | 100 | 1 | 1 | P | 1 | 34 | Isch | Occipital, substance blanche pariétale, putamen, noyau caudé |
| 18 | N | 69 / F | 100 | 3 | 2 | P | 2 | 60 | Isch | Frontal, temporal, parietal, corona radiata, putamen, noyau caudé |
2.2
Description de l’étude
Il s’agit d’un essai clinique randomisé contrôlé monocentrique en double insu comprenant 2 groupes de patients présentant une NS gauche : un groupe bénéficiant de la rééducation par AP et un groupe témoin. Le critère de jugement principal de l’étude était l’amélioration fonctionnelle dans les actes de la vie quotidienne après rééducation et mesurée par la mesure de l’indépendance fonctionnelle (MIF) . Ce score a été utilisé dans un essai clinique non randomisé évaluant l’efficacité d’une orthèse de tronc dans la rééducation de la NS chez deux groupes de patients . Ces auteurs ont montré, à 6 mois d’évolution, une différence statistiquement significative entre les scores moyens des 2 groupes (différence moyenne = 24 ; n = 11). Sachant que dans cette étude précédente, le critère de jugement MIF avait un écart-type de 10 unités, pour avoir 90 chances sur 100 au moins de mettre en évidence une différence de 25 points entre les réponses moyennes des deux groupes (avec un risque d’erreur de première espèce au plus égal à 5 %), il faudra inclure au minimum 9 sujets par groupe (c’est-à-dire : 1–β = 0,90 ; β = 0,10 ; α = 0,05 et Δ = 25 ; n = σ 2 × M/ Δ 2 = 100 × 54/625 = 8,6, soit au moins 9 sujets).
Une randomisation par bloc a été réalisée avec une distinction de deux niveaux de sévérité du déficit selon la gravité initiale de la NS évaluée par les tests d’inclusion : NS sévère : déficit présent à tous les tests d’inclusion, score au test de Schenkenberg et al. supérieur à 50 % de déviation et score de BIT ≤ 55 ; NS modérée : déficit présent à certains tests d’inclusion (de 1 à 4), score au test de Shenkenberg et al. compris entre 11 et 50 % de déviation et score de BIT > 55.
Il s’agit d’une étude en double insu : les examinateurs réalisant l’évaluation (G.R., S.L., E.M.) ignoraient si le patient inclus a bénéficié d’une AP ou non. Ils étaient distincts des examinateurs réalisant la tâche d’exposition aux lunettes prismatiques ou aux verres neutres (Y.R., S.J.C., L.P.). Par ailleurs, la procédure en double insu a été facilitée par le fait que les patients avec NS ne sont pas conscients de la perturbation induite par la déviation prismatique et ne présentent pas les réactions végétatives attendues lors de l’apparition d’erreurs motrices au début du port de prismes (cf. infra et ), ce qui permet de les affecter au groupes « prisme » et « témoin » à leur insu. De plus, cela permet aux investigateurs réalisant les évaluations de ne pas recevoir d’informations de la part des patients, qui pourraient dégrader le double insu en simple insu.
La randomisation par bloc et le tirage au sort répartissant les patients dans le groupe « prisme » ou « témoin » ont été réalisés par monsieur Denis Pélisson, directeur de l’équipe ImpAct, du centre de recherche en neurosciences de Lyon. Une randomisation à 2 niveaux a été réalisée : à un premier niveau, par la sélection des patients dans le groupe « prisme » ou « témoin », puis à un 2 e niveau, par la sélection des patients selon la gravité de la NS initiale à partir du score BIT, afin que le ratio patients atteints d’une négligence sévère et patients atteints d’une négligence modérée soit comparable dans les deux groupes.
Tous les patients ont donné leur consentement pour la participation à cette étude. La procédure expérimentale a été approuvée par le Comité consultatif de protection des personnes dans la recherche biomédicale Lyon B le 5 juin 2001 (dossier 2001-040 B). Les hospices civils de Lyon ont été le promoteur de cette étude, enregistrée le 2 août 2001 sous le numéro 2001/0294 . Le financement de l’étude a été assuré par l’ Inserm , les hospices civils de Lyon et l’ université Claude-Bernard – Lyon-1 .
2.3
Paramètres de l’étude
Les référentiels spatiaux et la précision des pointages vers une cible visuelle (réalisés sans rétroaction visuelle) ont été mesurés de l’inclusion du patient jusqu’à six mois afin de suivre leur évolution au cours de la récupération des patients. Une double mesure a de plus été réalisée, avant et après chaque séance d’exposition, afin de quantifier les effets consécutifs de l’adaptation prismatique.
Le critère de jugement d’efficacité thérapeutique principal est le score fonctionnel obtenu à partir de l’échelle de mesure de l’indépendance fonctionnelle (MIF) . Le critère secondaire est le score total du Behavioural Inattention Test (BIT) , reflétant la sévérité de la NS. La mesure du critère de jugement principal a été réalisée à 4 reprises : en pré-test et en post-tests à 1 (M1), 3 (M3) et 6 mois (M6) après la première séance d’AP. Pour la batterie BIT, deux évaluations ont été réalisées en pré-test et en post-tests à 6 mois ; aucune évaluation intermédiaire n’a été réalisée en cours de suivi afin de limiter l’effet confondant d’un apprentissage lié à la répétition des tests.
2.4
Adaptation prismatique et paramètres sensori-moteurs
Dans le groupe « prisme », l’AP a été obtenue par le port d’une paire de lunettes produisant une déviation optique du champ visuel de 10° vers la droite (OptiquePeter.com). Les verres prismatiques étaient composés de deux verres courbes point par point de 5° chacun, ajustés à une monture glacier avec des œillères latérales, afin d’éviter l’accès à la vision non décalée. Ces prismes couvraient un champ visuel total de 105° dont chaque champ monoculaire représentait 75° et le champ visuel binoculaire central 45°.
Pendant l’exposition prismatique, le patient devait réaliser 80 mouvements de pointage rapides en direction de cibles visuelles situées à 10 degrés à droite ou à gauche par rapport au milieu de son corps, alternées de façon pseudo-aléatoire. En dépit de l’instruction répétée de réaliser des mouvements rapides, la vitesse de mouvement des patients cérébrolésés reste généralement assez lente pour autoriser une rétroaction visuelle et les erreurs produites ne reflétaient pas toujours l’amplitude de la déviation optique ou le stade de l’adaptation ( Fig. 2 ). Cette vitesse restait cependant compatible avec le développement d’une adaptation sensori-motrice vraie en limitant les composantes stratégiques de la compensation . Les mouvements de pointage étaient réalisés avec une pause d’environ 30 secondes après chaque série de 20 permettant de favoriser une augmentation des erreurs au début de la série suivante. Durant l’exposition, le patient ne voyait pas la position initiale de la main, qui entrait dans le champ visuel entre le tiers et la moitié de son mouvement , afin de favoriser un codage proprioceptivo-visuel du mouvement . La durée de l’exposition prismatique était comprise entre 6 et 10 minutes. Les patients du groupe « témoin » réalisaient cette tâche visuo-motrice dans les mêmes conditions mais avec le port d’une paire de lunettes placebo, équipée de verres neutres de même poids et composées de deux verres prismatiques de 5 degrés collés en opposition et ne produisant aucune déviation optique ( ; OptiquePeter.com). Chaque patient a effectué la tâche d’exposition (avec lunettes prismatiques ou verres neutres) à 4 reprises : à j0 (Expo1), à j + 7 (Expo2), à j + 14 (Expo3) et à j + 21 (Expo4). Toutes les séances d’exposition ont été réalisées dans les mêmes conditions et avec les mêmes opérateurs.